血液融化设备通常包括血液融化箱、血浆融化箱、冰冻血浆解冻箱、冷冻血浆干式解冻仪,用于对临床血浆或血液进行加热、解冻,广泛应用与临床一线。本文为大家科普血液融化设备注册要求及审查要点,方便医疗器械注册企业更好规划产品研制及注册申报工作。
血液融化设备通常包括血液融化箱、血浆融化箱、冰冻血浆解冻箱、冷冻血浆干式解冻仪,用于对临床血浆或血液进行加热、解冻,广泛应用与临床一线。本文为大家科普血液融化设备注册要求及审查要点,方便医疗器械注册企业更好规划产品研制及注册申报工作。
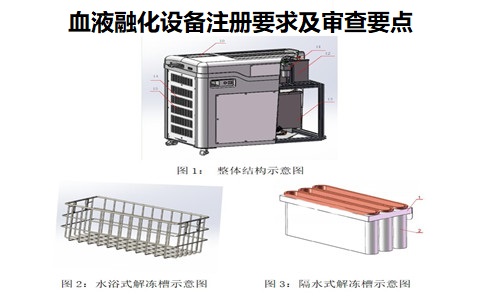
1.血液融化设备组成结构与预期用途:
血液融化设备通常由加热水箱、解冻槽、循环管路、进水管、排水管、控制箱等组成。分为水浴式、隔水式。用于对临床血浆或血液进行加热、解冻。
根据解冻水箱中解冻槽(解冻夹、解冻篮)的不同可以分为水浴式和隔水式。水浴式结构解冻过程中解冻血袋与热水直接接触,隔水式结构解冻过程中解冻血袋与热水进行隔离,两者不直接接触。
不同生产企业的产品,在结构上存在一定差异,可以与本部分描述不完全一致,组成部分的名称也不限于文中描述。
2. 血液融化设备产品技术要求的主要性能指标
产品技术要求应按照《医疗器械产品技术要求编写指导原则》的规定编制。解冻温度主要参考《血站技术操作规程(2019版)》和《临床输血技术规范》制定。如《血站技术操作规程(2019版)》要求,冰冻红细胞存储温度:≤-120℃(20%甘油),≤-65℃(40%甘油);解冻为:37~40℃恒温水浴融化。《临床输血技术规范》要求,冰冻血浆存储温度:≤-20℃;解冻为:37℃水浴融化。冷沉淀存储温度:≤-20℃;解冻方式参考冰冻血浆。
2.1.产品型号规格及其划分说明
产品可按结构组成、技术参数、预期用途等划分为不同型号和规格。
若有产品有多个型号,应提供型号间的主要差异对比表。
若含有软件,应按照《医疗器械软件注册技术审查指导原则》的要求,明确相应信息,如软件的名称、型号规格、发布版本、版本命名规则等。
2.2 解冻性能:
2.2.1 最大解冻容量:在申请人声称的摆放方式下,最大的血袋数量。
2.2.2 升温时间:预热完成后,加入最大数量冰冻血袋后,温度重新上升到设定解冻温度的时间,升温时间应符合申请人的规定。
2.2.3 解冻温度:
冷冻血浆:37℃;
冰冻冷沉淀:37℃;
冰冻红细胞:37~40℃。
温度的均匀性、波动范围应符合申请人的规定。
2.3 水位监控功能:
应有水位监测装置,当水位低于申请人要求时,应停止加热并发出异常提示。
2.4 显示功能
水位、温度等显示范围及误差。
2.5 温度保护功能:
应提供至少一个独立的超温保护装置,该装置应在不超过最高设定温度+2℃动作,停止加热,并提供连续的听觉和视觉提示。
2.6 隔水功能(隔水式适用)
解冻过程中,解冻槽的隔水部件不应漏水。
2.7 摆动功能(若适用)
摆动幅度、摆动频率应符合申请人的规定。
2.8 清洗消毒功能。
若产品具有清洗或消毒功能,应明确清洗流程,消毒方式、消毒参数。
2.9 噪声
产品工作噪声应≤65dB(A)。
2.10 软件
明确软件的功能、访问控制等要求,且应与说明书中的功能描述一致。
2.11网络安全
数据接口和用户访问控制要求。
明确软件的功能、访问控制等要求,且应与说明书中的功能描述一致。
2.12 安全性能
电气安全应符合GB 4793.1、GB 4793.6的要求。
电磁兼容应符合GB/T18268.1 的要求。
2.13 其他
产品具有的其他特定功能,应制定相应的指标。如二维码扫描功能等。
3.医疗器械注册单元划分
应按照《医疗器械注册与备案管理办法》、《医疗器械注册单元划分指导原则》要求,着重考虑产品的技术原理、结构组成、性能指标、适用范围等因素进行综合判定。