接着为大家科普有关包类医疗器械注册的要求,考虑到包类医疗器械注册产品实质是组件的组合和部分加工工序,组件在很大程度上决定了包类医疗器械注册要求,因此,本文来说说包类注册对组件有哪些要求,包类医疗器械能包含药物吗等等。
接着为大家科普有关包类医疗器械注册的要求,考虑到包类医疗器械注册产品实质是组件的组合和部分加工工序,组件在很大程度上决定了包类医疗器械注册要求,因此,本文来说说包类注册对组件有哪些要求,包类医疗器械能包含药品吗等等。
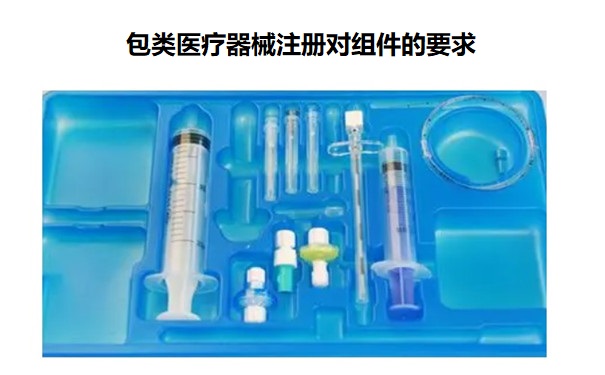
包类医疗器械注册对组件的要求:
包类医疗器械注册产品的组件可包含医疗器械、非医疗器械,医疗器械组件可以是已经取得医疗器械注册证的产品,也可以是未取得医疗器械注册证的产品。
参考国家药监局已发布的《一次性使用产包产品注册审查指导原则》,组件应包含医疗器械注册申请人在其申报的生产地址生产及获得医疗器械注册证的组件,且该产品的管理类别必须是包内组件的最高管理类别。即二类的包类医疗器械,注册人自己生产的组件应是第二类医疗器械,不能是第一类医疗器械。
组件不应含有药物(如乙醇、碘、灌洗创口用生理盐水等)及含有消毒剂的医疗器械(如碘伏棉球、含有消毒液的消毒刷等)。