人是组织的根本,是医疗器械注册质量管理体系中最重要的要素。对于医疗器械注册质量管理体缺陷来说,多数缺陷项的根本原因也是归结到人这个要素。本文从合规的角度,说说医疗器械注册质量管理体系核查对人员的要求。
人是组织的根本,是医疗器械注册质量管理体系中最重要的要素。对于医疗器械注册质量管理体缺陷来说,多数缺陷项的根本原因也是归结到人这个要素。本文从合规的角度,说说医疗器械注册质量管理体系核查对人员的要求。
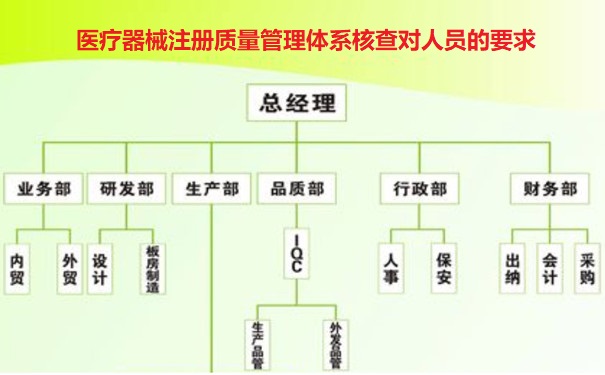
医疗器械注册质量管理体系核查对人员的要求
1.组织机构
医疗器械注册申请人应当建立与医疗器械研发、生产相适应的管理机构,明确各部门职责,确保设计开发和技术转换合理并可追溯。
2.人员
医疗器械注册申请人应当配备适当数量并具有相应的研发、生产和质量控制人员,人员应当具有与申报注册产品相适应的专业知识和工作技能。
3.关键人员
管理者代表、生产负责人、质量负责人、技术负责人、产品放行审核人等关键人员应当熟悉申报注册产品的关键质量控制、关键生产操作要求。
4.自检人员
医疗器械注册申请人提交自检报告的,质量检验部门应当配备足够数量的专职检验人员。检验人员的教育背景、技术能力应当与产品检验工作相匹配。检验人员、审核人员、批准人员等应当经申请人依规定授权。
更多医疗器械注册相关疑问或需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络,联系人:叶工,电话:18058734169,微信同。