《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号)第八条:第一类医疗器械实行备案管理,第二类、第三类医疗器械实行注册管理。境内第二类医疗器械由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。本文为大家介绍云南第二类医疗器械注册流程、时间和申报资料要求。
引言:《医疗器械监督管理条例》(国务院令第739号)第十三条:第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实行产品注册管理。第十六条:申请第二类体外诊断试剂产品注册,注册申请人应当向所在地省、自治区、直辖市人民政府食品药品监督管理部门提交注册申请资料。 《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号)第八条:第一类医疗器械实行备案管理,第二类、第三类医疗器械实行注册管理。境内第二类医疗器械由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。本文为大家介绍云南第二类医疗器械注册流程、时间和申报资料要求。
一、云南第二类医疗器械注册流程:
云南第二类医疗器械注册流程与其他省市基本一致,包括企业前期准备、医疗器械质量管理体系建设、产品研发定型、制造与质量保证能力具备、医疗器械注册检验、医疗器械注册申请、省药监局技术审评和注册质量管理体系考核、补正、获得医疗器械注册证、申请医疗器械生产许可证这些关键事项。
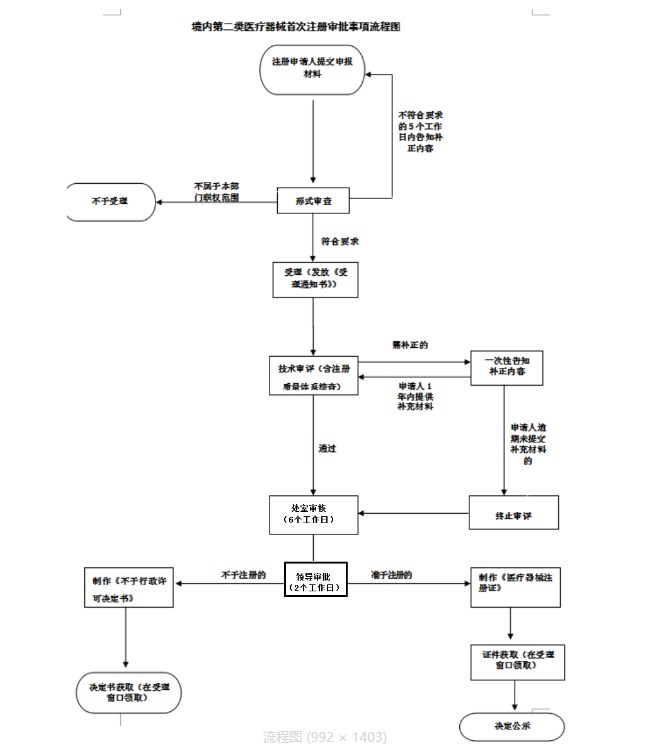
药监局医疗器械注册审评审批流程如下:

云南第二类医疗器械注册流程图如下:
二、云南第二类医疗器械注册时间
昨日与云南省医疗器械注册审评审批领导交流,云南省药监局于2022年推出加快云南医药审批20条,致力于优化医疗器械注册审评审批流程,提高云南第二类医疗器械注册审评审批效率。
尽管不同产品对应的医疗器械注册时间存在较大差异,但是主管领导的努力,及企业和第三方医疗器械注册服务机构的专业度,将帮助企业缩短产品注册时间,提高医疗器械注册上市效率。
三、云南第二类医疗器械注册申报资料要求
云南第二类医疗器械注册申报资料主要包括如下:
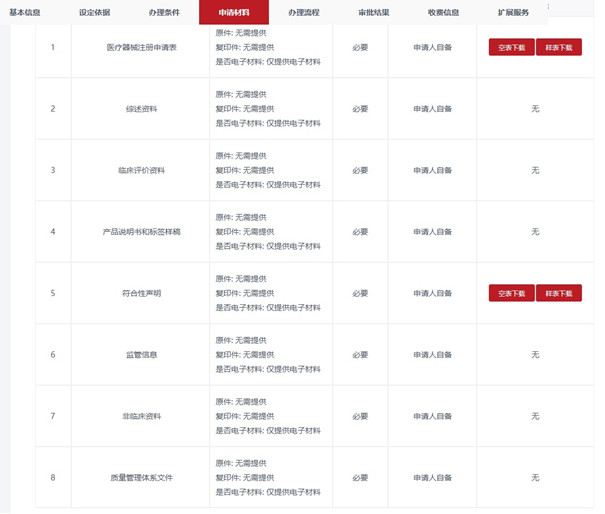
但考虑到国家局2022年开始推行新的医疗器械注册申报资料要求及文件目录结构,预计云南第二类医疗器械注册申报资料在不久的将来会与其它省市趋于一致。
更多有关云南第二类医疗器械注册服务需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络。联系人:叶工,电话:18058734169,微信同。