近日,为认真落实江苏省省委省政府、省市场监督管理局、省药品监督管理局关于优化审评服务与营商环境的有关要求,进一步加强对我省第二类医疗器械产品注册申报的指导服务,帮助医疗器械注册申请人提升注册申报的质量和效率,江苏省药监局审评中心梳理统计2023年第二类有源医疗器械拟上市注册申报资料的常见问题,供广大注册申请人参考。
近日,为认真落实江苏省省委省政府、省市场监督管理局、省药品监督管理局关于优化审评服务与营商环境的有关要求,进一步加强对我省第二类医疗器械产品注册申报的指导服务,帮助医疗器械注册申请人提升注册申报的质量和效率,江苏省药监局审评中心梳理统计2023年第二类有源医疗器械拟上市注册申报资料的常见问题,供广大注册申请人参考。
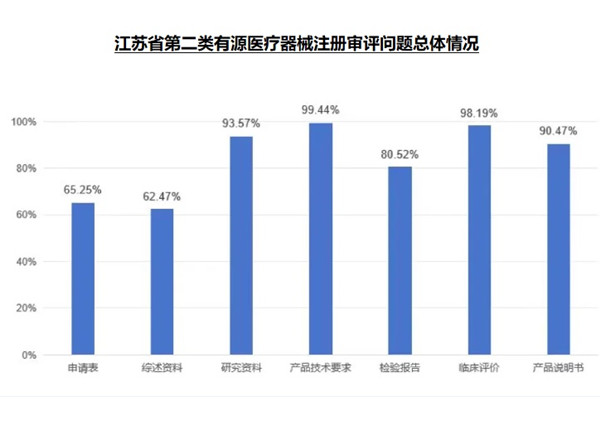
2023年江苏省药监局审评中心共计接收第二类有源医疗器械拟上市注册625件,发补率近100%,常见问题主要集中在申请表、综述资料、研究资料、产品技术要求、检验报告、临床评价和产品说明书等七部分(详见下图)。其中,
申请表发补率约为65.25%
综述资料发补率约为62.47%
研究资料发补率约为93.57%
产品技术要求发补率约为99.44%
检验报告发补率约为80.52%
临床评价发补率约为98.19%
产品说明书发补率约为90.47%
如有江苏省第二类有源医疗器械注册咨询服务需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络,联系人:叶工,电话:18058734169,微信同。