蒙古国卫生部药品和医疗器械司负责诊断药品和医疗器械注册和审查工作,蒙古医疗器械注册的法规依据是蒙古国政府于2010 年6月1日发布的《药品和医疗器械法》。

一、蒙古国医疗器械注册模式
不同于我国对医疗器械注册审批流程,医疗产品和医疗设备不需要在蒙古注册。采购机构进出口药品、医疗器械,应当取得《药品、医疗器械进口许可证》。进口许可证应当载明药品、医疗器械的名称、种类、剂量、数量、生产企业名称、国境口岸和日期。
诊断工具包(Diagnostic Kits)必须根据蒙古卫生部2019年9月9日第A295号命令“关于批准药品和物质注册条例”。诊断用医疗产品的注册程序类似于药品的注册程序。
二、蒙古医疗器械注册申请条件
进口药品、生物修复、药用原料和医疗器械(以下简称“进口药品和医疗器械”)的组织必须符合下列基本要求。
A) 必须有储存药品和医疗设备的仓库;
B) 必须有一名从有执照提供医学教育的学校毕业的医务专业人员,他将从事药品和医疗器械的质量认证、储存和分发活动;
C) 进口药品必须在国家药品注册中心注册;而且
D) 医疗器械必须有技术质量认证文件,药用原料必须符合质量要求。进口药品、医疗器械许可证的有效期不得超过1年。出口药品和医疗器械药品、生物修复、药用原料和医疗器械的出口和转口许可证由药品、生物修复和治疗质量控制办公室在人类医药部门理事会的评估基础上颁发。
三、蒙古国医疗器械注册审批流程
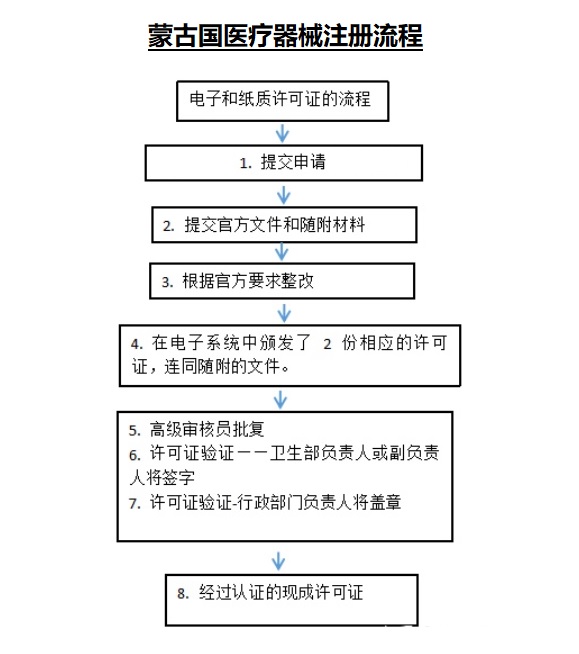
在进口许可证申请中,应当附有下列文件。
2.2.1. 与该药品或医疗器械的制造商、出口机构或持牌经销商签订的销售合同;
2.2.2. 合同规定进口货物的发票;
2.2.3. 在进口医疗器械时,应提供保证满足国际标准组织(ISO)的制造商和产品要求的证书。
更多有关蒙古国医疗器械注册服务需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络,联系人:叶工,电话:18058734169,微信同。