近日,国家药监局披露2024年7月国产第三类医疗器械注册审评用时,及进口第二类医疗器械注册审评用时和进口第三类医疗器械注册审评用时,其中进口第二类医疗器械注册?审评阶段平均用时343天,第三类医疗器械注册审评阶段平均用时291天,从统计数据来看,第三类医疗器械注册审评事件并不比第二类医疗器械注册审评用时更多。
近日,国家药监局披露2024年7月国产第三类医疗器械注册审评用时,及进口第二类医疗器械注册审评用时和进口第三类医疗器械注册审评用时,其中进口第二类医疗器械注册审评阶段平均用时343天,第三类医疗器械注册审评阶段平均用时291天,从统计数据来看,第三类医疗器械注册审评事件并不比第二类医疗器械注册审评用时更多。
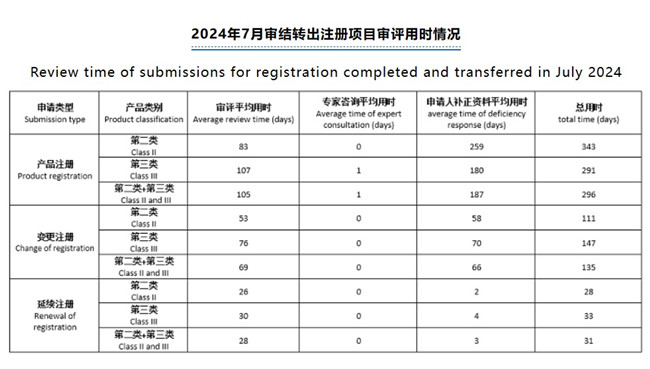
国家药监局2024年7月医疗器械注册审评用时
备注:
1.本表涉及时间均为工作日。
The time in this table is working days.
2.补正资料平均用时=补正资料总用时/相关项目审结转出总数量
average time of deficiency response = total time of deficiency response /total number of completed and transferred submissions with deficiencies.
3.总用时=审评平均用时+专家咨询平均用时+补正资料平均用时
Total time = average review time+ average time of expert consultation + average time of deficiency response.
4.第二和第三类产品平均用时=第二类和第三类产品用时/第二类和第三类产品总数量
Average time for Class II and III products = total treview time of class II and III products/the total number of class II and III product submissions.
5.应急审评用时不在统计范围内
Time of emergency review is out of the scope of this statistics.
此外,从上图中也可以看到,进口第二类医疗器械变更注册审评阶段平均用时是111天,第三类医疗器械注册审评阶段平均用时是147天;进口第二类医疗器械延续注册审评阶段平均用时是28天,第三类医疗器械延续注册审评阶段平均用时是33天。