牙科种植体(系统)是近年最热门的齿科第三类医疗器械注册?产品之一。2024年9月29日,国家药监局发布了《牙科种植体(系统)注册审查指导原则(2024年修订版)》,借这个契机,为大家带来牙科种植体(系统)产品技术要求及注册审查要点,一起看正文。
牙科种植体(系统)是近年最热门的齿科第三类医疗器械注册产品之一。2024年9月29日,国家药监局发布了《牙科种植体(系统)注册审查指导原则(2024年修订版)》,借这个契机,为大家带来牙科种植体(系统)产品技术要求及注册审查要点,一起看正文。
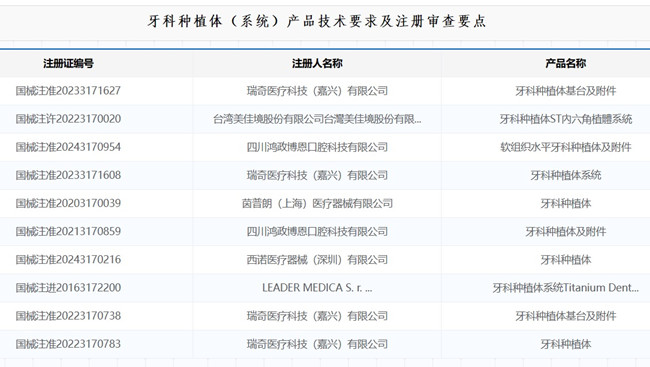
一、牙科种植体(系统)产品技术要求
产品技术要求需符合相关国家标准、行业标准和有关法律、法规的相应要求。在此基础上,注册申请人需根据产品的特点,制定保证产品安全、有效的技术要求。产品技术要求中试验方法需依据有关国家标准、行业标准、国际标准制订,或经过确认与验证。牙种植体(系统)产品可参考YY 0315《钛及钛合金牙种植体》、YY/T 0520《钛及钛合金材质牙种植体附件》、YY 0304《等离子喷涂羟基磷灰石涂层 钛基牙种植体》、YY/T 0521《牙科学 种植体 骨内牙种植体动态疲劳试验》相关标准制定相应性能要求。
1.产品型号/规格及其划分的说明
列表说明产品的型号、规格,明确产品型号、规格的划分说明。明示产品结构组成信息。提供各型号产品的结构图并标识关键尺寸。
2.性能指标
产品技术要求的主要性能指标需包括以下适用内容:
2.1各部位几何尺寸及允差,需包括直径、长度、圆锥角。
2.2牙种植体与种植体基台的配合性能,包括牙种植体与种植体基台内连接配合及偏差、牙种植体与种植体基台配合间隙、螺纹偏差。
2.3表面性能,包括外观、表面缺陷、软组织水平牙种植体颈部粗糙度。
2.4清洁。
2.5机械性能,包括抗扭性能、紧固性能。
2.6无菌。
2.7细菌内毒素。
2.8涂层性能(如适用),涂层抗拉粘结强度、微观形貌(平均厚度、表面粗糙度、涂层形貌、孔隙率)。
3.检验方法
产品的检验方法需根据技术性能指标设定,优先采用公认的或已颁布的标准检验方法,包括推荐性标准,需注明相应标准的编号和年代号。自建检验方法需提供相应的方法学依据及理论基础,同时保证检验具有重复性和再现性,必要时可附相应图示进行说明,文本较大的可以附录形式提供。
4.附录
产品各组件化学成分及符合标准信息、显微组织/低倍组织、涂层材料信息(涂层材料成分、HA含量及结晶度、杂质元素含量极限、钙磷原子比、其他结晶相)、产品表面元素分析、疲劳极限,以资料性附录形式体现。
二、牙科种植体(系统)产品注册审查要点
根据产品特性及临床预期风险,开展物理和机械性能验证,可参考YY 0315、YY 0304、YY/T 0520、YY/T 0521相关标准。对于表面采用喷砂酸蚀、阳极氧化等加工而成的钛及钛合金常规种植体系统接受限值可直接参考上述标准中明确接受阈值,对于相关标准中尚无接受阈值的性能要求,建议进行对比研究。研究项目包括但不限于:
1.配合性能,需提交种植体(系统)的配合性能验证资料。需考虑牙种植体与种植体基台连接处的配合、配合间隙、螺纹偏差、敲击固位及莫氏锥度/圆锥固位精度(如适用)、拔出力(如适用)、敲击力(如适用)、冷焊效果(如适用)性能研究资料,建议不少于5组,对于敲击固位、莫氏锥度/圆锥固位研究建议与已上市相同固位形式产品进行对比研究。
2.力学性能,需结合产品结构设计提交抗扭性能、紧固扭矩、旋动扭矩、自攻性能(适用于自攻型牙种植体)、轴向拔出力(适用于即刻种植)研究资料。
3.疲劳极限:需结合产品结构设计及配合使用的情形,选取申报产品中力学性能最差产品参照YY/T 0521《牙科学 种植体 骨内牙种植体动态疲劳试验》开展疲劳极限研究,并对试验结果的可接受性进行分析,可选择与已上市产品疲劳性能对比分析,建议注意申报产品和同品种产品疲劳性能测试条件的一致性。对于小直径种植体疲劳极限较低,仅可满足前牙区使用的情况,建议一并选择后牙区可用最小直径种植体(系统)开展疲劳极限或较大载荷值的疲劳验证研究。对于特殊设计的种植体(系统),如穿颧种植体,需结合临床应用形式选取合适的疲劳试验模型,提供试验模型设计依据,并对试验结果进行可接受性分析。
4.耐腐蚀性能:若种植体系统包含不同种类的金属组件且以前未见相似的用法时,需进行申报产品的耐腐蚀性能研究。申报产品的配合方式在目前境内已上市产品中有相同的用法时,可不进行该项研究。
5.表面性能:需明确申报产品的表面处理方法,包括喷砂酸蚀、阳极氧化及其他表面处理,提供表面处理工艺验证及表面形态特征的研究验证资料,一般需包括表面形貌、微观结构、表面化学分析、涂层均匀性、涂层剥脱/磨损、溶解性、种植体颈部等,对于通过表面处理/表面涂层增加牙科种植体表面粗糙度的情形,还需考虑牙科种植体根部粗糙度、孔洞结构、孔隙率等,具体如下:
5.1对于陶瓷涂层,需提供以下信息:涂层材料粉末颗粒大小及粒度分布、化学成分及化学性质分析、X射线衍射图谱;涂层制备工艺、后处理工艺及其特点,包括涂层的平均孔径、孔隙率、表面涂层和截面扫描电镜照片、厚度和公差、所有晶相的百分比、X射线衍射图谱、磨损、脱落或脱离、溶解性、涂层抗拉强度、涂层粘结强度。
5.2对于金属涂层,需提供以下信息:涂层材料的化学成分及涂层自身的化学成分、涂层厚度及孔隙率、孔隙截距、表面形态特征、晶相及非晶相比例及分布、种植体涂层表面和截面扫描电镜照片、涂层磨损、脱落或脱离和溶解性。
5.3对于喷砂处理,需提供以下信息:喷砂处理种植体表面特征、所使用喷砂粒子的化学成分、喷砂工艺特征(如压力、喷砂时间、喷砂角度等)、喷砂粒子残留、用于去除喷砂粒子的物质的理化特性及其工艺过程、种植体表面分析及种植体表面微观结构分析。
5.4对于酸蚀处理,需提供以下信息:种植体表面处理所用酸蚀剂的化学成分,处理工艺,处理后种植体表面酸蚀层的形态特征、表面化学组成分析及分析方法、扫描电镜照片。应当控制酸蚀剂的残留量。
5.5对于盐涂层,需提供以下信息:化学成分、涂层厚度、孔径及孔隙覆盖率、粗糙度、表面形貌、磨损特性、沉积盐量、溶解性、亲水接触角、沉积盐量对牙槽骨组织的影响。
5.6其他处理
若对种植体表面进行其他技术处理,对于具有特殊宣称(如亲水性、利于细胞黏附、提高初期稳定性等)、或首次上市的表面处理工艺,还需针对宣称提供相应的证据及支持性资料,提供该表面处理工艺对产品安全有效性的研究验证资料。
6.稳定性能:牙科种植体系统需开展初期稳定性研究,观察牙科种植体稳定系数、骨结合骨吸收水平,评估牙科种植体初期稳定性水平。对于表面处理方式、结构形式较已上市种植体存在差异的,如特殊规格种植体(直径小于3.25mm、长度小于7mm)、特殊表面处理、即刻负重及新的应用技术等,需提交长期稳定性评估资料,建议观察周期不少于6个月。
7.化学/材料表征研究
牙科种植体(系统)中各组件需说明材料的选择依据、材料来源,对所选用的材料应当进行质量控制并符合相关材料标准要求,材料需具有稳定的供货渠道以保证产品质量,外购材料需提供材料的供方名录。需提供各组件材料化学及力学性能验证资料,如化学成分、显微组织、晶粒度、涂层成分、表面元素分析、相对杂质含量及其上限、溶解性、金属材料力学性能(抗拉强度、0.2%规定非比例延伸强度、断裂伸长率、断面收缩率(如适用)、弹性模量(如适用))、陶瓷材料弯曲强度及抗冲击韧性、复合材料的弯曲强度及弹性模量。